Abstrak
Selama beberapa dekade terakhir, berbagai upaya telah dilakukan untuk mengganti katalis logam dengan alternatif yang lebih murah dan berlimpah di bumi atau untuk sepenuhnya menyingkirkan logam dari reaksi cross-coupling sambil mempertahankan efisiensi tinggi dalam transformasi target. Namun, studi lanjutan sering kali mengungkap peran pengotor logam dalam proses katalitik. Dengan demikian, pengotor logam aktif dapat menyebabkan kesalahan interpretasi mekanistik, dan ini dapat memicu arahan penelitian yang keliru dan menyebabkan masalah reproduktifitas yang parah. Preseden penting dari efek pengotor dalam reaksi cross-coupling didokumentasikan dengan baik dalam literatur. Menariknya, kekeliruan ini telah berulang kali terjadi selama bertahun-tahun karena kurangnya studi mekanistik menyeluruh dan skema studi penelitian yang tepat untuk mengidentifikasi efek pengotor. Di sini, kami mengusulkan pedoman untuk menjelaskan katalis sebenarnya dari transformasi katalitik masa depan, yang bertujuan untuk mengungkap mekanisme yang benar dan membantu menyingkirkan peran pengotor dalam proses katalitik baru. Meskipun pedoman ini terutama berfokus pada masalah yang terkait dengan jejak logam transisi, pedoman ini juga menawarkan dasar untuk penelitian katalis yang lebih umum.
Katalis logam mulia sangat efisien dan serbaguna sehingga membentuk persepsi kita tentang katalisis. Namun, katalis ini juga memiliki kekurangan, termasuk biaya tinggi, dampak lingkungan, dan, dalam beberapa kasus, efek kesehatan yang merugikan. Banyak sekali penelitian telah dilakukan untuk meminimalkan pemuatan katalis logam mulia dengan mengoptimalkan kondisi reaksi dan ligan atau menggantinya dengan logam atau bahan organik yang lebih melimpah. Dalam dua arah penelitian terakhir ini, masalah penting harus ditangani untuk membangun transformasi katalitik yang dapat direproduksi: “katalisis kontaminasi.” Ini terjadi ketika senyawa yang ditambahkan secara tidak sadar bertanggung jawab atas transformasi tersebut.
Dalam konteks yang lebih luas, pengotor logam transisi dapat memiliki dampak yang berbeda pada katalisis. Bahkan dalam jumlah minimal, logam dapat bertindak sebagai inhibitor dan inisiator dalam banyak bidang kimia; oleh karena itu, pengaruhnya terhadap proses katalitik harus dipertimbangkan. Dalam polimerisasi radikal, penggunaan inisiator berbasis logam sudah mapan, [ 1 ] dan secara historis, pengotor logam transisi menyebabkan penemuan katalis polimerisasi Ziegler–Natta berbasis Zr dan Ti yang efisien. [ 2 , 3 ] Di antara proses yang dikatalisis logam transisi dalam sintesis organik, reaksi Nozaki–Hiyama–Kishi adalah contoh penting dari transformasi yang dipengaruhi pengotor. Dalam proses ini, sejumlah kecil NiCl2 dalam reagen kromium ditemukan sebagai katalis sebenarnya yang bertanggung jawab atas transformasi tersebut. Peran pengotor Ni sebagai katalis aktif dalam reaksi siklopropanasi dijelaskan oleh Chen dan rekan kerja, [ 4 ] memberikan penjelasan untuk irreproducibility dari metode “bebas logam” asli yang dikembangkan oleh Franzen dan Wittig pada tahun 1960-an. [ 5 ] Pengotor dapat bertindak tidak hanya sebagai katalis tetapi juga sebagai inhibitor, seperti yang ditunjukkan oleh kasus Pb dalam siklopropanasi Simmons-Smith. [ 6 ] Banyak dari preseden tonggak sejarah ini dirangkum dengan sangat baik dan dibahas secara rinci oleh Thomé, Nijs, dan Bolm, bersama dengan contoh katalitik lainnya (vide infra). Oleh karena itu, kami tidak menguraikan latar belakang sejarah secara rinci. [ 7 ] Di luar preseden ini, ada beberapa contoh efek pengotor logam transisi di bidang elektrokimia [ 8 – 10 ] dan fotokatalisis. [ 11 ] Namun, bidang-bidang ini berada di luar cakupan utama perspektif ilmiah kami dan tidak akan dibahas secara ekstensif. Meskipun demikian, beberapa aspek pedoman ini mungkin masih berlaku dan berguna di area penelitian ini.
Singkatnya, katalisis kontaminasi memainkan peran ganda dalam penelitian. Dalam beberapa kasus, ketika diidentifikasi dan dikelola di awal proses penelitian, hal itu dapat mengarah pada penemuan yang sangat bermanfaat, seperti pengembangan katalis industri yang efisien untuk transformasi katalitik yang lebih ekonomis dan berkelanjutan [ 12 ] dengan menghilangkan jejak pengotor penghambat. Di sisi lain, mewujudkan metode alternatif dan yang lebih baik tetap menjadi tantangan yang signifikan. Semakin besar penyimpangan dari metode asli, semakin penting untuk memberikan bukti mekanistik eksperimental dan komputasional untuk konsep baru. Selain itu, potensi partisipasi logam asli sebagai kontaminan jejak dalam prosedur baru harus dipertimbangkan dengan cermat untuk memastikan reproduktifitas dan interpretasi mekanistik yang wajar. Dalam hal ini, beberapa saran praktis dapat ditemukan dalam catatan yang relevan, [ 13 ] tetapi pedoman yang lebih rinci untuk analisis dan pencegahan efek pengotor tidak ada dalam literatur. Dengan demikian, kami bertujuan untuk mengumpulkan masalah utama dan memberikan panduan untuk meminimalkan masalah reproduktifitas dan salah tafsir dalam katalisis.
1 Pengurangan, Penggantian, dan Penghilangan Katalis
Di antara reduksi, penggantian, dan penghilangan, opsi pertama adalah yang paling mudah dicapai dalam hal reproduktifitas dan ketahanan. Dalam konteks ini, banyak metode yang dikatalisis paladium dilakukan secara efisien dengan jumlah paladium “homeopatik” ppb–ppm, [ 14 – 16 ] misalnya, dengan kompleks paladium yang berkarakterisasi dengan baik [ 17 – 19 ] dan nanopartikel dengan berbagai ukuran. [ 20 – 24 ] Dalam kasus seperti itu, masuk akal untuk berasumsi bahwa jalur mekanistik yang sama relevan dalam reaksi tersebut.
Penggantian katalis logam transisi yang diketahui dengan katalis alternatif merupakan tugas yang lebih menantang, tergantung pada jenis reaksinya. Dalam pendekatan ini, kelayakan penggantian harus dibuktikan, dengan mendefinisikan peran katalis baru yang tepat dalam siklus katalitik. Untungnya, ada contoh-contoh di mana logam yang relatif murah dan berkelanjutan seperti nikel [ 23 , 25 – 30 ] dan tembaga [ 31 – 35 ] telah terbukti bertindak sebagai katalis dalam spektrum reaksi kopling silang yang luas, menggantikan logam yang lebih mahal.
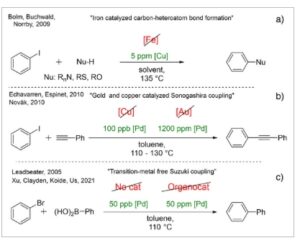
Namun, dalam kasus tertentu, pengotor dalam katalis dan aditif yang digunakan berpartisipasi dalam reaksi. Contoh representatif dan ilustratif dari efek ini adalah upaya penggantian tembaga dengan besi dalam reaksi penggandengan pembentukan ikatan karbon-heteroatom. [ 36 – 38 ] Tak lama setelah pengungkapan penggandengan “katalis besi” ini, Bolm dan Buchwald mengungkapkan bahwa katalisis kontaminasi disebabkan oleh kadar ppm tembaga yang ada dalam besi. Akibatnya, garam besi ultra-murni tidak mengkatalisis reaksi (Gambar 1a ). [ 39 ] Kesimpulan yang bermanfaat dari penelitian ini adalah bahwa penggandengan dapat dicapai secara efektif dengan kadar ppm katalis tembaga. [ 40 ]
Gambar 1
Buka di penampil gambar
Presentasi PowerPoint
Katalisis kontaminasi dalam literatur.
Demikian pula, kopling Sonogashira yang dikatalisis tembaga [ 41 , 42 ] dan emas [ 43 ] dari alkuna terminal dan aril halida terdokumentasi dengan baik dalam literatur. Namun, dalam kedua kasus, tingkat ppm/ppb pengotor paladium [ 44 ] diidentifikasi sebagai spesies katalitik aktif, yang mungkin disebut sebagai katalis kontaminasi (Gambar 1b ). [ 45 , 46 ]
Kotoran mungkin ada dalam katalis, basa, atau bahkan dalam pelarut atau peralatan. Misalnya, dalam penelitian kami sebelumnya, [ 46 ] kami menunjukkan, dalam kasus reaksi Sonogashira, bahwa batang pengaduk yang sebelumnya digunakan dalam reaksi yang dikatalisis Pd dapat mentransfer cukup paladium ke dalam reaksi lain untuk mencapai konversi lengkap, bahkan setelah dibersihkan (bukan dengan aqua regia). Batang pengaduk sebagai sumber kontaminasi teknis dipelajari secara mendalam oleh Janiak [ 47 ] dan Ananikov [ 48 ] dan rekan kerja, yang membuat pernyataan ilmiah yang didukung dengan baik tentang peran kotoran logam yang diangkut oleh aksesori laboratorium umum ini.
Sasaran yang paling memuaskan namun paling menantang secara sintetis adalah penghilangan total logam mulia dari proses katalitik. Pendekatan ini juga telah dicoba sebelumnya dalam reaksi cross-coupling, [ 49 ] tetapi setelah contoh pertama reaksi Suzuki bebas paladium, Leadbeater dan rekan menilai kembali hasil mereka sebelumnya (Gambar 1c ) dan menunjukkan bahwa bahkan kadar paladium ppb mampu mengkatalisis reaksi dalam kondisi optimal. [ 50 ] Temuan ini mengubah masalah menjadi keuntungan: sistem katalitik hiperaktif dan metode yang berguna ditemukan untuk pembentukan ikatan C─C dengan pemanfaatan sejumlah kecil katalis paladium.
Karena manfaat yang potensial, jenis perkembangan ini tetap menjadi fokus studi katalitik, dan para peneliti mengalami masalah, tantangan, dan kesulitan yang sama. Baru-baru ini, reaksi penggandengan tipe Suzuki–Miyaura yang dikatalisis amina telah dikembangkan (Gambar 1c ). [ 51 ] Telah ditunjukkan bahwa turunan anilin yang difungsikan secara khusus dapat berfungsi sebagai katalis untuk reaksi ini. Mengingat pentingnya temuan ini, komunitas katalisis tertarik untuk menggunakan jenis katalis baru ini, yang mengarah pada aplikasi sintetis. [ 52 ] Sayangnya, kontaminasi paladium yang terjadi selama persiapan katalis sangat sulit dihilangkan menggunakan banyak teknik. Akibatnya, temuan ini harus ditinjau kembali dan diklarifikasi. [ 53 , 54 ]
Contoh-contoh di atas menunjukkan bahwa identifikasi katalisis kontaminasi merupakan hal yang sangat penting. Ini merupakan tugas yang paling krusial dan sulit, dan kecurigaan yang sehat harus selalu dipertahankan, dan tanda-tanda peringatan harus diperiksa. Di bawah ini, kami menguraikan indikasi paling umum yang harus selalu diperiksa baik secara eksperimental maupun komputasional untuk mengidentifikasi kasus potensial katalisis kontaminasi.
1.Tanda-tanda Kemungkinan Efek Kontaminasi
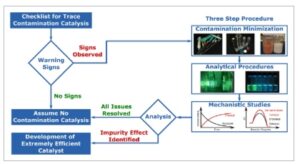
Mengenali kapan harus meneliti peran katalis sangatlah penting (Gambar 2 ). Berdasarkan contoh-contoh sebelumnya, fenomena berikut dapat mengindikasikan katalisis kontaminasi.
Reaksi yang baru dikembangkan ini melibatkan katalis yang terkenal. Transformasi yang sangat mirip telah dikembangkan dalam kondisi yang sebanding, menggunakan bahan awal yang sama dan menghasilkan produk yang serupa, dengan pemanfaatan katalis logam yang terdefinisi dengan baik .
2. Mencocokkan cakupan reaksi dengan preseden literatur. Saat menyelidiki cakupannya, mungkin menjadi jelas bahwa ada korelasi dalam reaktivitas pasangan substrat ( misalnya , efek gugus donor elektron dan gugus penarik elektron pada substrat serupa ) .
3. Suhu tinggi diperlukan untuk transformasi Tampaknya menjadi pengamatan umum bahwa pada suhu yang jauh lebih tinggi, bahkan sejumlah kecil kotoran katalis dapat menjadi efektif
4. Reaktivitas yang tidak terduga pada reaksi tertentu. Ada beberapa kelompok bahan awal yang kinerjanya lebih baik daripada kelompok lain, atau contoh di mana reaksi berlangsung jauh lebih cepat atau lebih lambat dari biasanya. Hal ini dapat mengindikasikan adanya katalis yang ditambahkan secara tidak sengaja. Salah satu sumber yang mungkin adalah aditif yang ditambahkan secara berlebihan, termasuk pelarutnya. Sumber kontaminasi katalis lainnya termasuk peralatan, khususnya batang pengaduk .
5.Profil pengotor yang analog dengan reaksi yang diketahui. Profil pengotor suatu reaksi sama atau sangat mirip dengan reaksi yang diketahui dikatalisis oleh logam lain. Reaksi sampingan dapat menjadi tanda katalisis yang tidak disengaja .
6. Perhitungan teoritis menunjukkan penghalang yang luar biasa tinggi. Hambatan yang dihitung tidak konsisten dengan laju reaksi yang diamati secara eksperimen pada suhu yang digunakan Nomor telepon
7. Perbedaan antara prediksi komputasi dan hasil eksperimen.
Metode komputasi terkini memberikan prediksi yang kuat dalam hal tren relatif aktivitas. Penyimpangan besar dalam tren tidak boleh terjadi jika mekanisme yang tepat dipertimbangkan
Gambar 2
Buka di penampil gambar
Presentasi PowerPoint
Metode dan pedoman untuk menjelaskan spesies yang aktif secara katalitik.
Jika semua poin yang disebutkan di atas negatif, seseorang dapat melanjutkan dengan asumsi bahwa kontaminasi tidak relevan dalam reaksi yang diberikan. Namun, jika kecurigaan tetap ada, prosedur tiga langkah direkomendasikan untuk secara efektif meminimalkan risiko salah tafsir aktivitas katalis yang disebabkan oleh katalisis kontaminasi.
1.Diperlukan untuk membuat pengaturan laboratorium dan memilih bahan awal yang secara sistematis meminimalkan semua sumber potensial kontaminasi. Kami menyediakan deskripsi terperinci tentang praktik laboratorium yang sesuai di bagian “Minimalisasi Kontaminasi.”
2.Dengan pengaturan sintetis yang biasa dan sistem katalitik yang terkontaminasi minimal, penting untuk menilai tingkat kontaminasi secara keseluruhan melalui prosedur analitis. Kami telah mengumpulkan dan memberikan petunjuk terperinci untuk memperoleh hasil yang dapat diandalkan di bagian “Prosedur Analitis.”
3.Dengan memiliki akses ke pengaturan reaksi dan tingkat kontaminasi yang sesuai, seseorang dapat mempelajari pengaruh kontaminasi pada reaksi dan mekanismenya baik secara eksperimental maupun komputasional. Untuk membantu hal ini, kami telah menyusun saran yang dapat langsung diterapkan di bagian “Pemeriksaan Mekanistik Sistematis” untuk memandu pembaca.
Prosedur tiga langkah yang dijelaskan di atas dapat membantu pengembangan metodologi di masa mendatang dan berfungsi sebagai referensi bagi para peninjau dan editor di masa mendatang yang mungkin memiliki masalah. Untuk mendukung prosedur tiga langkah ini, kami telah menyediakan “Daftar Periksa Katalis Kontaminasi” terperinci dengan petunjuk langkah demi langkah dalam Informasi Pendukung.
3 Minimalisasi Kontaminasi
3.1 Umum
Masalah utama yang umum adalah peralatan dan kemurnian laboratorium secara umum. Laboratorium tempat logam transisi telah digunakan secara luas dapat menjadi sumber potensial kontaminasi dan harus dihindari. Lebih jauh, kotak sarung tangan sering kali merupakan ruang penyimpanan dan penggunaan katalis yang sangat aktif dari berbagai jenis; oleh karena itu, kotak sarung tangan harus dihindari atau, jika tidak memungkinkan, diperlakukan dengan sangat hati-hati.
Kotoran logam sisa pada bejana reaksi, jalur vakum, dan kotak sarung tangan dapat berasal dari reaksi sebelumnya dan bahkan air keran. [ 11 , 55 , 56 ] Oleh karena itu, kami umumnya menyarankan penggunaan peralatan gelas baru, terutama batang pengaduk, tetapi peralatan dapat dicuci dalam beberapa kasus. Peralatan gelas harus direndam seluruhnya dalam Aqua Regia yang baru disiapkan semalaman, kemudian harus dibilas dengan air suling dan direndam dalam air suling selama 30 menit. Setelah dibilas dengan air suling, disarankan untuk mengeringkan dalam oven yang bersih. [ 57 ] Bejana polietilen dapat dimurnikan dengan asam nitrat. [ 58 ] Untuk jalur vakum, kami sarankan pembersihan menyeluruh dengan menggunakan metode di atas, bersama dengan tabung dan konektor baru. Untuk spatula dan sendok, merupakan praktik yang baik untuk menandai dan memisahkannya untuk setiap bahan dan tingkat kemurnian, atau menggunakan yang plastik baru sekali pakai.
Dengan peralatan murni di tangan, kita harus memastikan bahwa komponen utama (berdasarkan berat) semurni mungkin. Ini biasanya meliputi pelarut, aditif/basa, dan bahan awal. Pelarut harus dimurnikan menggunakan metode yang tepat, seperti distilasi di bawah atmosfer inert dan dengan agen pengering, tergantung pada sifat dan kemurnian yang dibutuhkan. Pelarut dengan kemurnian tertinggi yang tersedia secara komersial dapat digunakan tanpa pemurnian lebih lanjut. Untuk aditif dan basa, kemurnian yang dapat diterima dapat dipastikan dengan mendapatkan kemurnian tertinggi yang tersedia dari pemasok yang dapat diandalkan dan menyimpannya dalam kondisi yang tepat untuk mencegah kontaminasi. Bahan awal harus dimurnikan menggunakan teknik seperti rekristalisasi, kromatografi kolom, atau sublimasi, dengan kemurnian dikonfirmasi melalui kromatografi cairan kinerja tinggi (HPLC) atau spektrometri massa (MS). Jika perlu, spektrometri massa plasma yang digabungkan secara induktif (ICP-MS) dapat digunakan untuk mendeteksi elemen jejak di luar komponen yang diharapkan dari senyawa yang diberikan. Untuk deskripsi yang lebih komprehensif mengenai teknik pemurnian dan praktik terbaik, kami sarankan untuk menggunakan literatur yang tersedia mengenai pemurnian, [ 59 ] yang menyediakan metode terperinci untuk memastikan reagen dan bahan dengan kemurnian tinggi.
Secara umum, logam yang berbeda sering ditemukan bersama-sama dalam proses produksi bahan kimia anorganik karena kelimpahan alaminya. Oleh karena itu, garam logam sederhana dengan kemurnian yang dapat diterima untuk kimia organik (>95%) tidak sesuai untuk studi katalitik. Setiap kemungkinan kontaminasi harus diminimalkan untuk komponen reaksi kritis ini, dan sumber logam harus memiliki kemurnian tertinggi yang tersedia (>99,99%). Perlu dicatat bahwa bahan dengan kemurnian 99,999% masih mengandung 10 µg g −1 pengotor. Bergantung pada pengaturan reaksi, hal ini saja dapat memasukkan 10 ppm katalis potensial yang tidak diketahui, yang dapat mengalihkan rute reaksi dalam banyak kasus. Penggunaan persen massa (b/b %) sebagai ukuran kemurnian dapat menyesatkan, karena bahan dengan berat molekul tinggi dapat mengandung jumlah pengotor yang jauh lebih besar. Misalnya, cesium karbonat sangat berguna karena kelarutannya yang relatif baik dalam pelarut organik. Namun, ia mengandung lebih dari tiga kali jumlah pengotor dibandingkan dengan padanan natriumnya dengan b/b % yang sama.
Bahkan dengan upaya yang dilakukan untuk memastikan kemurnian peralatan dan material, kontaminasi tidak dapat dikesampingkan, dan tidak cukup hanya membandingkan kondisi baru dengan protokol yang ada. Reaksi kosong tanpa kandidat katalis harus dilakukan untuk memastikan bahwa reaksi tidak berlangsung tanpa katalis yang dimaksud (reaksi latar belakang/katalis).
Khususnya untuk reaksi yang menantang seperti itu, reproduktifitas harus dipastikan. [ 60 , 61 ] Pertama, reproduktifitas antar-batch harus dikonfirmasi (menggunakan batch baru bahan awal untuk katalis, substrat, dan pelarut dari pemasok yang berbeda). Selanjutnya, ketahanan harus divalidasi dalam kondisi yang se-independen mungkin, sebaiknya dalam kelompok penelitian yang independen. Idealnya, hasilnya harus direplikasi menggunakan bahan awal yang paling tidak maju secara sintetis dan bersumber secara lokal di laboratorium lain.
Namun, perlu diingat bahwa “katalisis kontaminasi” tidak dapat sepenuhnya dikesampingkan bahkan dalam skenario ini.
3.2 Kemurnian “Katalis Logam Pengganti”
Jika transformasi kimia yang mapan membutuhkan katalis berbasis logam yang sangat mahal dan/atau beracun, mungkin lebih baik menggunakan katalis yang lebih murah atau lebih baik, yang disebut “katalis logam pengganti”. Namun, logam-logam ini sering kali berasal dari kelompok logam yang sama, dengan asumsi bahwa kesamaan kimianya dapat dimanfaatkan melalui pengoptimalan katalis yang lebih baik.
Beberapa logam transisi muncul bersamaan di alam dan bahkan dapat diekstraksi dari bijih yang sama. Pemurnian dalam proses dapat menjadi sulit karena kesamaan kimia antara logam-logam ini. Masalah ini dapat menjadi lebih buruk: ketika kemunculan alami logam serupa tidak cukup tinggi bagi produsen logam untuk mengekstrak dan menghilangkannya, maka logam-logam ini hadir sebagai pengotor. Fakta ini dapat menyebabkan masuknya kontaminan logam yang tidak diharapkan ke dalam campuran reaksi oleh katalis logam utama. Sayangnya, data komprehensif tentang kontaminasi logam yang umum pada unsur-unsur tersebut tidak tersedia bagi pengguna; kami telah mengumpulkan beberapa sumber untuk mewakili kompleksitas masalah ini. Misalnya, sebagian besar logam golongan platina berasal dari penambangan nikel. Logam-logam ini diekstraksi bersama-sama, dan langkah-langkah awal dalam proses pemurnian untuk mendapatkan logam platina melibatkan penghilangan nikel dan kemudian tembaga. Selanjutnya, melalui sebagian besar pemurnian larutan, perak, emas, paladium, rutenium, osmium, platina, iridium, dan rodium dipisahkan dalam urutan ini. [ 62 ] Mirip dengan logam platinum yang diekstraksi bersama, kobalt juga diekstraksi dari bijih tembaga dan nikel. [ 63 ] Emas dengan kemurnian tinggi dapat mengandung Pd, Fe, Cu, dan Ag dalam kisaran 10 µg g −1 . Jumlah pastinya sangat bervariasi karena ketidakhomogenan makroskopis yang diakibatkan oleh titik leleh yang berbeda. [ 64 , 65 ] Logam murni lainnya (Hg, Ga, In, Sn, Zn, Al, Ag, Au, Cu) yang digunakan sebagai standar untuk skala suhu dapat mengandung beberapa pengotor. [ 66 ] Besi dapat mengandung tembaga, timbal dan seng, kalsium, aluminium, dan mangan. [ 39 , 67 , 68 ] Litium karbonat (98+%) juga dapat mengandung tembaga, besi, dan nikel, sebagai tambahan terhadap logam alkali dan alkali tanah yang diharapkan, pada konsentrasi ratusan mg kg −1 . [ 69 ]
Dalam konteks ini, kita selalu dapat menduga adanya kontaminasi silang di antara logam-logam ini, dan untuk menghindari keterlibatan “katalis logam pengganti”, sangat disarankan untuk memeriksa lembar data kemurnian pemasok, dan jika perlu, menganalisis komponen minor katalis logam dengan ICP-MS. Dengan ini, kita tidak dapat mengesampingkan semua efek yang tidak diinginkan, tetapi kita dapat mempertimbangkan skenario katalitik lainnya dan mengidentifikasi titik kritis mekanisme reaksi.
Sebagai catatan tambahan mengenai logam mulia, kita harus mempertimbangkan bahwa logam platinum dan paladium merupakan bagian dari kehidupan sehari-hari melalui katalis otomotif, dan konsentrasinya dapat melebihi 100 µg kg −1 dalam debu jalan di beberapa jalan yang ramai. [ 70 ] Bahkan kentang dapat mengandung sejumlah µg kg −1 platinum dan sejumlah ng kg −1 rodium. [ 71 ] Jadi, bukan hanya bahan kimia komersial yang dapat mengontaminasi reaksi kita, tetapi kita dapat memasukkan jejak logam dari banyak sumber jika bahan-bahan tersebut tidak ditangani dengan tepat.
3.3 Kemurnian Organokatalis Potensial
Mengembangkan organokatalis yang baik sangat bermanfaat untuk banyak aplikasi, terutama dalam pengaturan industri (farmasi). Namun, dalam persiapan organokatalis, sangat penting untuk menghindari penggunaan katalis logam transisi apa pun, terutama yang dapat digunakan sebagai katalis dalam reaksi target. Lebih jauh, sumber bahan kimia harus dipilih dengan cermat, karena jejak logam sering terbawa melalui beberapa langkah dalam sintesis multi-langkah. Setelah disintesis, pemurnian kandidat katalis merupakan tugas yang penting tetapi menantang.
Teknik kromatografi merupakan metode yang terkenal dan bermanfaat untuk pemurnian bahan kimia organik. Di sisi lain, teknik ini tidak direkomendasikan sebagai satu-satunya metode pemurnian. Dalam kasus di mana komponen yang sangat kecil mungkin ada, terdapat risiko tinggi terjadinya ko-elusi, karena interaksi dengan senyawa organik yang diinginkan dapat menghambat proses pemisahan.
Di sisi lain, rekristalisasi yang cermat, di mana kristal berukuran sedang terbentuk, merupakan teknik yang efisien untuk mencapai kemurnian katalis yang memadai. Distilasi dan sublimasi juga dapat dilakukan, tetapi biasanya bukan solusi praktis di bawah massa sampel tertentu.
Selain teknik pemurnian umum, pemulung logam transisi dapat diterapkan untuk mengurangi kandungan unsur-unsur ini. Namun, metode ini memiliki keterbatasan yang harus dipertimbangkan. Yaitu, proses-proses ini harus dioptimalkan dengan hati-hati untuk aplikasi yang diberikan, dan bahkan kemudian, konsentrasi logam residu dalam kisaran ppm mungkin masih ada. [ 72 ] Ketahanan ini disebabkan oleh dua kendala yang tersisa. Pertama, jika senyawa organik memiliki kemampuan untuk membentuk bahkan kompleks yang lemah dengan logam, kemungkinan besar akan ada dalam bentuk kompleks, mengingat konsentrasi senyawa organik adalah orde besaran lebih tinggi. Kedua, campuran tersebut mungkin mengandung kompleks pra-terbentuk yang sangat stabil, yang hanya sedikit dipengaruhi oleh pemulung.
Pemurnian bahan organik juga dapat dilakukan melalui metode elektrokimia dengan cara mengendapkannya pada elektroda. Pendekatan ini juga dapat berguna dalam analisis kualitatif, karena logam yang diendapkan terkonsentrasi pada elektroda dan dapat dianalisis. [ 73 ]
Jika katalis organik adalah bahan polimer, pemurniannya yang tepat merupakan tugas yang sangat sulit. Salah satu pendekatan yang mungkin adalah menggunakan GPC. Dengan menggunakan teknik ini untuk pemurnian fotokatalis polimer yang diduga, Kosco dan rekan-rekannya berhasil mengurangi tingkat Pd dari polimer mereka, yang disintesis dengan kopling Suzuki, dari 1170 ppm hingga di bawah batas deteksi mereka sebesar 1 ppm. [ 74 ]
Molekul dengan gugus fungsi yang lebih polar lebih rentan terhadap akumulasi pengotor logam. Akibatnya, obat-obatan dan asam amino rentan terhadap kontaminasi logam dalam jumlah tinggi, termasuk besi, nikel, tembaga, dan kromium. [ 75 – 78 ]
4 Prosedur Analitis
ICP merupakan alat utama untuk mengidentifikasi kemungkinan kontaminan logam transisi, tetapi persiapan sampel dapat terabaikan jika sampel tidak disiapkan dengan hati-hati. Di bawah ini, kami memberikan rekomendasi untuk persiapan sampel yang tepat.
Cawan yang dibersihkan dengan baik dan asam dengan kemurnian tinggi sangat penting untuk persiapan sampel yang tepat. Bejana pencernaan harus dicuci terlebih dahulu dengan air ultramurni (18,2 MΩ cm −1 ) menggunakan asam encer (asam nitrat dan/atau asam klorida) untuk pencucian asam.
Sampel harus menjalani pencernaan lengkap dengan perlakuan asam berbantuan gelombang mikro. [ 79 ] Untuk ini, asam nitrat pekat dengan kemurnian tinggi dan asam klorida harus digunakan dalam rasio aqua regia terbalik (cc. HNO 3 dan cc. HCl 3:1). Asam nitrat mengoksidasi komponen organik sampel, sementara asam klorida memastikan bahwa logam transisi tetap dalam larutan.
Larutan yang diperoleh melalui pencernaan gelombang mikro harus dilarutkan ke dalam air ultramurni (18,2 MΩ cm −1 ). Larutan yang dihasilkan harus dianalisis dengan instrumen ICP-OES atau ICP-MS. Bergantung pada konsentrasi logam, salah satu atau kedua teknik harus digunakan.
Kalibrasi eksternal harus dilakukan menggunakan larutan standar ICP satu atau beberapa elemen, dan kurva kalibrasi tiga hingga empat titik harus diukur untuk menghitung kandungan logam dalam sampel. Jika jumlah sampel memungkinkan, sebaiknya lakukan dua atau tiga pengukuran ICP paralel dengan tiga persiapan sampel independen.
Untuk konsentrasi yang mendekati batas deteksi, percobaan lonjakan harus dilakukan, dan pemulihan lonjakan harus dilaporkan.
Alat lain yang berguna dalam pencarian logam transisi adalah pemanfaatan sensor fluoresensi. Pengukuran kuantitatif pada tingkat ppm dapat dicapai untuk logam tertentu menggunakan sensor dan peralatan yang relatif sederhana. Namun, kekurangannya adalah beberapa sensor bersifat khusus untuk unsur tertentu, jadi seseorang harus tahu apa yang harus dicari. Ada beberapa metode untuk mendeteksi logam transisi melalui fluoresensi. [ 80 – 83 ] Aplikasi paladium yang lebih berfokus pada kimia organik telah dikembangkan oleh kelompok penelitian Koide. [ 84 – 87 ]
Meskipun NMR, seperti yang digunakan oleh ahli kimia sintetis, tidak terlalu efektif dalam mengidentifikasi pengotoran yang sangat kecil yang tidak diketahui, NMR dapat memberikan beberapa petunjuk. [ 73 ] Perhatikan puncak-puncak kecil dan cobalah untuk melacak asal-usulnya. Jalankan NMR untuk inti-inti yang tampaknya tidak ada, seperti fosfor, nitrogen, atau fluorin. Dalam beberapa kasus, ligan-ligan yang mengikat kuat mungkin ada dan terlihat oleh pengamat yang jeli.
4.1 Pemeriksaan Mekanistik Sistematis
Salah satu pendekatan yang mungkin untuk menentukan apakah kontaminasi logam (transisi) memainkan peran penting dalam transformasi tertentu adalah dengan mempelajari mekanisme reaksinya secara sistematis. Metode yang paling sering digunakan untuk tujuan ini adalah kinetika eksperimental atau komputasional, serta estimasi efek isotop dan substituen.
Secara konseptual, reaksi bebas kontaminasi dan reaksi yang disertai lonjakan harus dipelajari untuk menyingkirkan aktivitas katalitik kontaminan. Secara teknis, sistem yang sepenuhnya bebas kontaminasi tidak pernah dijamin secara eksperimental, meskipun kemurnian dapat diupayakan (lihat Bagian 3 ).
Untuk menyingkirkan kemungkinan bahwa reaksi tersebut didorong oleh pengotor, eksperimen kinetik yang ketat akan sangat berharga tetapi membosankan. Untungnya, banyak informasi dapat dikumpulkan dari eksperimen yang disederhanakan. Untuk perkiraan cepat, seseorang dapat memilih titik tertentu pada konversi antara (yaitu, hasil 70%) untuk perbandingan. Memantau reaksi dari waktu ke waktu dan membandingkan kurva hasil waktu dapat mengungkapkan kesamaan mekanistik. Sementara satu reaksi mungkin berlangsung lebih cepat, bentuk kurva mungkin memberikan wawasan yang berharga.
Percobaan spiking yang disebutkan di atas harus dilakukan dengan hati-hati, karena informasi mengenai jumlah katalis yang sebenarnya sering kali terbatas. Jika sudah terdapat terlalu banyak katalis yang ada dari matriks reaksi, menambahkan terlalu sedikit kontaminan yang diduga mungkin tidak akan memengaruhi hasil reaksi. Katalis kontaminasi dapat aktif pada skala ppm atau bahkan ppb. Oleh karena itu, spiking reaksi kosong dengan berbagai jumlah logam yang mencurigakan dari ppb hingga mol% rendah harus diperiksa. Bahkan dengan pendekatan yang hati-hati ini, penting untuk diingat bahwa efek sinergis dapat mempersulit reaksi melalui interaksi antara dua logam atau antara kontaminasi logam dan zat organik yang memiliki sifat khelasi.
4.2 Aspek Komputasi
Berbeda dengan pengaturan eksperimental, pendekatan komputasional menyediakan akses ke jalur katalis logam yang umum dan mekanisme alternatif yang diusulkan. Oleh karena itu, harus dibuktikan bahwa katalis yang disarankan jauh lebih efektif daripada kontaminan pada tingkat kontaminasi eksperimental semaksimal mungkin. Prosedur ini tunduk pada beberapa trik umum, [ 88 ] seperti persyaratan umum untuk analisis konformasi, [ 89 ] koreksi konsentrasi yang tepat, termasuk solvasi implisit dan, jika perlu, eksplisit, dan identifikasi keadaan istirahat dan langkah-langkah penentu laju untuk kedua mekanisme. [ 90 , 91 ]
Akan tetapi, beberapa masalah khusus muncul karena sifat masalah tersebut. Pertama, karena kontaminan hadir pada konsentrasi yang sangat rendah dalam satu mekanisme tetapi sama sekali tidak ada pada mekanisme lainnya, tinggi penghalang hanya dapat dibandingkan secara langsung jika konsentrasi dopan secara eksplisit diperhitungkan alih-alih menggunakan konsentrasi 1 mol dm −3 yang biasa . Kedua, karena reaktan yang tidak larut (yaitu, senyawa alkali padat) sering digunakan, perhatian khusus harus diberikan pada penanganannya. Idealnya, seseorang harus mempertimbangkan simulasi komputer dari antarmuka padat-cair melalui simulasi dinamika molekuler ab initio (AIMD). Sebagai pendekatan alternatif, perhitungan klaster-kontinum telah disarankan dan dilengkapi dengan penentuan AIMD dari struktur fase larutan. [ 92 ] Meskipun pendekatan ini memiliki ketelitian teoritis, studi komputasi yang melibatkan teknik-teknik ini jarang dapat dilakukan. Oleh karena itu, solusi yang lebih pragmatis tetapi perkiraan telah disarankan untuk memperkirakan energi bebas Gibbs dari aditif padat ini pada skala yang konsisten dengan perhitungan kimia kuantum. Salah satu pilihannya adalah menggabungkan siklus termodinamika dengan data eksperimen dan komputasi. [ 93 ] Meskipun pendekatan ini sangat mudah, pendekatan ini rentan terhadap kesalahan yang cukup besar karena spesies memiliki struktur elektronik yang sangat berbeda. [ 94 ] Pilihan lebih lanjut mungkin mencakup pendekatan komputasional murni terhadap siklus termodinamika, termasuk keadaan padat, fase gas, dan perhitungan pelarut implisit [ 93 ] atau ekstrapolasi untuk memberikan batas bawah energi bebas solvasi melalui model kluster ukuran yang meningkat, [ 95 , 96 ] Pada akhirnya, penggantian reaktan padat harus dicoba secara eksperimental untuk mendapatkan reaksi model yang dapat diikuti melalui spektroskopi fase homogen dan kimia komputasional juga.
Mengingat ketidakpastian yang timbul dari tantangan yang disebutkan di atas, kami sarankan untuk mempelajari efek substituen atau efek isotop kinetik jika berlaku. Efek substituen mungkin memberikan tren yang berbeda untuk kedua mekanisme tersebut. Oleh karena itu, jika transformasi yang ada dengan katalis lain mirip dengan metode yang baru dikembangkan, sangat disarankan untuk membandingkan kedua reaksi tersebut. Untuk tujuan ini, beberapa senyawa dari cakupan substrat reaksi lain dengan pola substitusi yang serbaguna harus dipilih. Kemudian, kinetika dan konversi kedua reaksi harus dibandingkan, bersama dengan estimasi komputasional yang sesuai. Pengukuran NMR atau GC dari campuran reaksi mentah disarankan untuk menghindari kesalahan tambahan dengan teknik pengerjaan.
Bahkan jika tidak ada reaksi analog yang bebas kontaminasi atau dikatalisis logam yang terdefinisi dengan baik, kami sarankan untuk mempertimbangkan kuantitas yang bergantung pada laju relatif karena tren lebih kuat berkenaan dengan masalah teknis daripada konstanta laju absolut. Hal yang sama berlaku untuk pengukuran dan perhitungan efek isotop kinetik, yang sangat diuntungkan dari pembatalan kesalahan.
5 Kesimpulan
Kami telah menyusun pedoman sebagai rekomendasi untuk pengembangan metodologi di masa mendatang, yang menekankan pentingnya penanganan material dan peralatan yang tepat, pemurnian, dan analisis produk untuk mencegah kesalahan interpretasi mekanistik. Kami menyadari bahwa mematuhi semua rekomendasi kami merupakan upaya yang berat, tetapi mematuhi pedoman yang disajikan dan melaporkan hasil yang sesuai akan sangat meningkatkan kredibilitas prosedur sintetis yang baru disarankan. Dengan mengatasi masalah kritis ini, peneliti dapat menghemat sumber daya yang berharga dengan mengidentifikasi dan mengatasi masalah terkait kontaminasi di awal penelitian mereka. Pada akhirnya, kami berharap bahwa pendekatan ini dapat mengubah kutukan efek pengotor menjadi berkah dalam mengidentifikasi sistem katalis yang baru dan sangat efisien dalam penelitian kimia. [ 97 ]
